肿瘤细胞与其周围基质(ECM)之间的多种自分泌和旁分泌有助于肿瘤细胞增殖,从而改变其微环境、生长、存活和转移特性。这些相互作用对于具有大量纤维化间质的癌症(如胰腺癌、三阴性乳腺癌、肉瘤、卵巢癌)异常重要。研究表明:基质活化会损害传统化学治疗药物的主动摄取且会促进癌细胞的肿瘤发生、治疗抵抗和转移扩散。因此,近年来,靶向肿瘤基质以改善药物递送结合标准护理疗法已成为一种有前途的治疗策略。LRRC15参与细胞-细胞和细胞-基质相互作用,由于其在间充质来源的肿瘤(如肉瘤、胶质母细胞瘤和黑色素瘤)中的过表达而成为有前途的抗癌靶点。艾伯维等药企巨头纷纷布局,但是该靶点在国内却相对冷门。如今,ADC赛道日渐拥挤,靶点布局同质化问题严重,差异化布局或是破局关键。LRRC15也许是一个不错的选择。
癌细胞与肿瘤微环境(TME)之间的相互作用在肿瘤的侵袭性方面发挥着重要作用。癌症相关成纤维细胞(cancer-associatedfibroblasts,CAF)是肿瘤微环境中研究最多的成分之一,其通过ECM沉积和重塑、免疫调节、促进血管生成和促进代谢等多种机制促进肿瘤发生及对治疗的耐受性。CAF在肿瘤微环境中被包括炎症因子、DNA损伤(继发于化疗或放疗)、生理应激和生长因子(FGF、PDGF和TGF-β)等多种刺激激活。研究发现TGF-β驱动的CAF基因特征在癌症进展和免疫治疗耐药性中发挥重要作用。
I型跨膜蛋白LRRC15(Leucine-rich repeat-containing protein 15)是LRR超家族的成员,被认为参与蛋白质-蛋白质和蛋白质-基质相互作用以及各种细胞过程的信号转导,受TGF-β调节。先前的研究表明,LRRC15在TGF-β驱动的CAF中高表达,而正常组织表达低。针对不同癌症类型的多项研究表明,转移性肿瘤中LRRC15 的表达升高。Klein等人通过对基因表达分析显示LRRC15是乳腺癌患者中许多显著上调的基因之一。在Cui等人最近的一项研究中,高LRRC15表达与骨肉瘤患者的转移、化疗反应差和总生存期较短有关。LRRC15的敲除减少了体内异种移植模型中卵巢癌细胞的转移性传播。除了在整合素信号传导中的潜在作用外,LRRC15最近已被证明通过调节Wnt/β-连环蛋白信号通路促进TNBC肿瘤迁移和侵袭。因此,LRRC15已成为针对CAF和TME的潜在靶点。

图1.(A)LRRC15结构示意图和(B)其通过激活粘着斑激酶信号传导促进癌症转移的作用
ABBV-085是由艾伯维公司研发的一种人源化抗LRRC15 ADC,毒素为MMAE,目前进展最快。研究表明在包括肉瘤、乳腺癌、肺癌、胰腺癌和胶质母细胞瘤(≥2+LRRC15 阳性)等多种癌症类型的临床前模型中显示出对ABBV-085治疗的有效性。
在ASCO 2019上,艾伯维公布了关于ABBV-085的一项I期研究的研究结果,78名患者接受单药剂量递增治疗(从0.3 至4.8mg/kg 每2 周给药一次),然后以3.6mg/kg进行剂量扩展。在骨肉瘤和未分化多形性肉瘤患者中发现了初步的抗肿瘤活性,与其他MMAE ADC相比,ABBV-085似乎是安全和可耐受的。
此外,ABBV-085与免疫检查点抑制剂的联合治疗也在临床前的癌症模型中显示出增强的抗肿瘤活性。这表明诸如ABBV-085 等LRRC15靶向疗法可能对免疫疗法耐药的患者具有令人鼓舞的治疗潜力。
蒽环类化疗药物显著提高了骨肉瘤患者的生存率,LRRC15-PNU由蒽环类衍生物PNU-159682与LRRC15 ADC偶联而成,对其在骨肉瘤临床前模型中的评估结果显示:LRRC15-PNU在骨肉瘤异种移植模型中治愈率在40-100%。
在2021 AACR上,Bicycle还公布了LRRC15靶向双环肽偶联药物BT1769的进展。国内齐鲁制药研发了靶向LRRC15/CD3的双抗QL315。
这一系列研究结果表明,LRRC15可能是治疗实体瘤的潜力股。
LRRC15是实体瘤治疗中一个重要且潜在可利用的靶点。与非恶性细胞相比,LRRC15在选定的间充质来源肿瘤中的差异表达能够实现靶向特异性蒽环类药和低毒性的功效。LRRC15未来可用于诊断和治疗目的,鉴定表达LRRC15的肿瘤组织将有助于确定LRRC15是否可以成为所涉及的肿瘤类型中更好的预测标志物和治疗靶点。
为了助力相关研究,ACROBiosystems开发了一系列LRRC15蛋白,可用于免疫、抗体筛选、细胞功能验证等多种应用场景。
此外,ACROBiosystems还提供ADC药物一体化解决方案,满足ADC药物从抗体制备,筛选到后期的生产质控全流程,协助加速ADC药物研发。

★ 蛋白均一结构及高纯度(>90%)经MALS验证
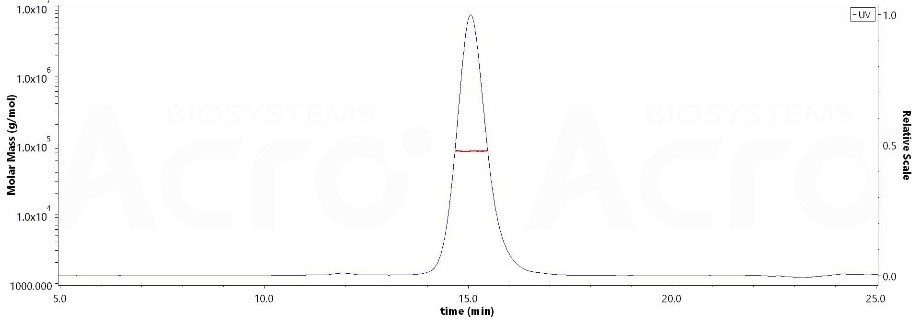
The purity of Human LRRC15, His Tag (Cat. No. LR5-H52H3) is more than 90% and the molecular weight of this protein is around 65-90 kDa verified by SEC-MALS.
★ 与抗体的结合活性经ELISA验证
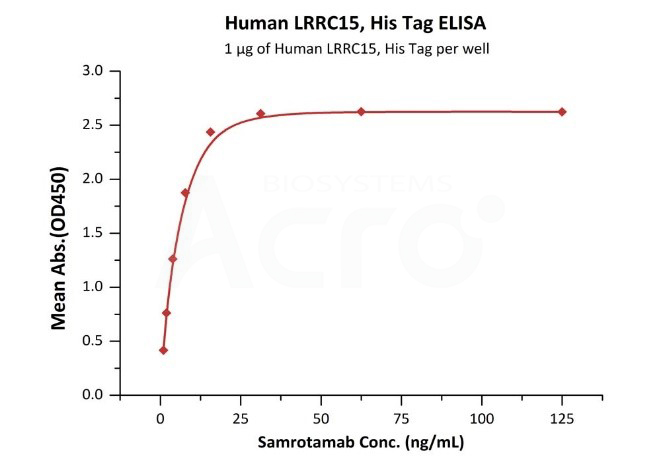
Immobilized Human LRRC15, His Tag (Cat. No. LR5-H52H3) at 10 μg/mL (100 μL/well) can bind Samrotamab with a linear rangeof 1-16 ng/mL (QC tested).
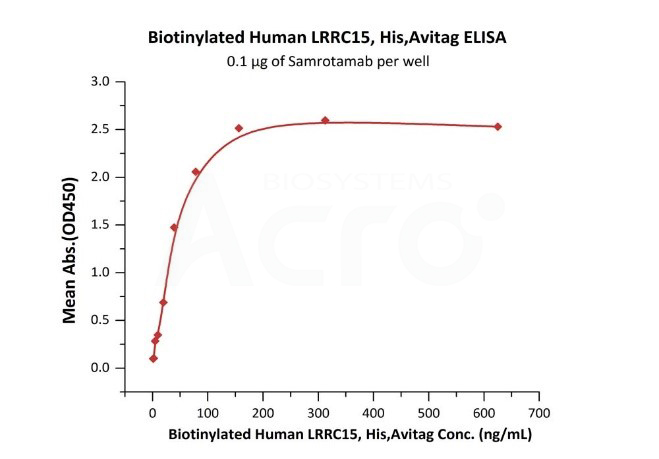
Immobilized Samrotamab at 1 μg/mL (100 μL/well) can bind Biotinylated Human LRRC15, His,Avitag (Cat. No. LR5-H82E4) with a linear range of 1-313 ng/mL (QC tested).
1.Ray U, Pathoulas CL, Thirusangu P, Purcell JW, Kannan N, Shridhar V.Exploiting LRRC15 as a novel therapeutic target in cancer. Cancer research. 2022 May 5;82(9):1675.
2.Tang H , Liu W , Xu Z , et al. Integrated microenvironment-associated genomic profiles identify LRRC15 mediating recurrent glioblastoma-associated macrophages infiltration[J]. Journal of Cellular and Molecular Medicine.


















 Star Ribbon预染蛋白Marker蛋白质标记物是生物研究和药物开发的重要组成部分。无论是用于蛋白质电泳还是western blot,我们的预染色蛋白质标记物帮助您快速确定目标蛋白质的分子量或评估转移效率。Fc受体蛋白治疗性抗体的功效取决于Fab片段及其对目标抗原的结合活性,还取决于Fc片段及其与关键Fc受体的相互作用。因此,在抗体工程中候选物必须针对一系列受体进行测试。探索我们的重组Fc受体蛋白质的全面收藏!
Star Ribbon预染蛋白Marker蛋白质标记物是生物研究和药物开发的重要组成部分。无论是用于蛋白质电泳还是western blot,我们的预染色蛋白质标记物帮助您快速确定目标蛋白质的分子量或评估转移效率。Fc受体蛋白治疗性抗体的功效取决于Fab片段及其对目标抗原的结合活性,还取决于Fc片段及其与关键Fc受体的相互作用。因此,在抗体工程中候选物必须针对一系列受体进行测试。探索我们的重组Fc受体蛋白质的全面收藏!


































 膜杰作
膜杰作 Star Staining
Star Staining















